

ご存知のように、癌の治療は、主に手術、抗癌剤、放射線、免疫療法などによってなされております。「活性化自己リンパ球移入療法」というのは免疫療法の1つで、癌細胞を攻撃する自分自身のリンパ球を体外でインターロイキン2とともに培養することにより活性化した後、体内に戻すことにより体の中の癌細胞を攻撃させ、癌を小さくしようという治療法です。平成17年6月現在で、この治療法を高度先進医療として承認を受けている施設は広島大学病院をはじめとして14施設あります(http://www.mhlw.go.jp/topics/0106/tp0601-1a.html)。
口腔の各器官は咀嚼、嚥下、発音などの重要な機能を有しており、根治的手術は重大な機能障害、ひいてはQOLの低下を招くことになります。そこで、当科では当初より口腔癌に対して抗癌剤と放射線による導入療法と、機能温存的手術を行ってきました。その経過の中で、活性化自己リンパ球を主とした免疫療法を導入療法に組み入れることにより、より優れた治療効果を得ることができることを明らかにするとともに、強い細胞傷害能を持つリンパ球の誘導方法についても検討してまいりました。それらの結果より得られた知見をもとに、最近では超選択的に挿入した動注カテーテルより抗癌剤や放射線と併用して活性化自己リンパ球を投与することにより、さらに優れた治療効果を挙げることができるようになり、約40%の症例では手術を受けずにすみ、手術を受けないといけない場合でも小さな手術で済ますことができ、口腔機能が良好に保たれております。さらに、われわれは唾液腺癌に対しても、分化・アポトーシス誘導による治療を試みてきており、腺様嚢胞癌に対し化学・放射線療法に加えこの活性化自己リンパ球移入療法を組み入れた免疫療法を施行したところ、癌が骨に置換し治癒した症例を経験しております。このような症例は他施設でも数例報告されておりますが、それらはいずれも活性化自己リンパ球移入療法がなされており、本療法の唾液腺癌への有用性が示唆されます。本療法は、自分自身のリンパ球を用いるため重篤な副作用は無く、今後、現在本院で臨床試験が行われているWT1ワクチンとの併用などにより、治療効果の更なる向上が期待されます。
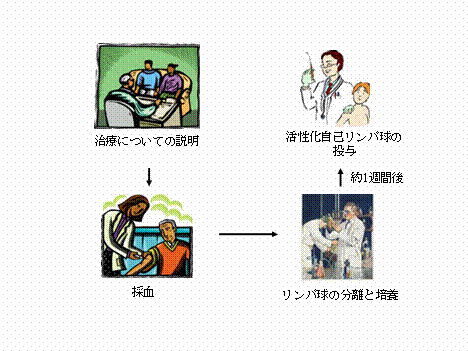
治療費は1回につき90,700円で、通常、1週間に1回のペースで、合計3〜4回施行します。
1. Yoneda
K, Yamamoto T, Ueta E, Osaki T: Induction of lymphokine-activated killer cells
with low-dose interleukin 2 and interferon-γ in oral cancer patients, J Clin
Immunol 12:289-299, 1992
2. Yoneda
K, Osaki T, Yamamoto T, Ueta E: Effects of tumour necrosis factor-alpha
(TNF-α), IL-1β and monocytes on lymphokine-activated killer (LAK) induction
from natural killer (NK) cells and T lymphocytes, Clin Exp Immunol 93:229-236,
1993
3. 米田和典,山本哲也,尾崎登喜雄:NKおよびT細胞におけるIL-2誘導シグナル伝達について,BIOTHERAPY 8:430-431,
1994
4. 植田栄作,米田和典,山本哲也,尾崎登喜雄:LAK+化学・放射線治療による上顎腺様嚢胞癌の分化誘導−腫瘍細胞の分化誘導とアポトーシス,BIOTHERAPY 9:451-452,
1995
5. 山本一彦,米田和典,山本哲也,立本行宏,尾崎登喜雄:LAK細胞と5-FUによる口腔扁平上皮癌株におけるapoptosis誘導,BIOTHERAPY 9:453-454,
1995
6. Yamamoto
T, Yoneda K, Osaki T, Yoshimura N, Akagi N: Longer local retention of adoptively
transferred T-LAK cells correlates with lesser adhesion molecule expression
than NK-LAK cells, Clin Exp Immunol 100:13-20, 1995
7. 米田和典,山本哲也,尾崎登喜雄:NKおよびT細胞におけるIL-2シグナル伝達,口科誌 45:143-151,
1996
8. Yoneda
K, Osaki T, Yamamoto T: IL-2 signalling in T and natural killer (NK) cells
associated with their class I-non-restricted killing activity, Clin Exp Immunol
106:179-186, 1996
9. Yamamoto
T, Yoneda K, Ueta E, Tatemoto Y, Osaki T: Combination adoptive immunotherapy
with chemoradiotherapy in oral carcinomas, Int J Clin Oncol 1:150-156, 1996
10. Ueta
E, Osaki T, Yamamoto T, Yoneda K: Induction of differentiation in maxillary
adenoid cystic carcinomas by adoptive immunotherapy in combination with
chemoradiotherapy, Oral Oncol 34:105-111, 1998
11. Yamamoto
T, Yonea K, Ueta E, Doi S, Osaki T: Enhanced apoptosis of squamous cell
carcinoma cells by interleukin-2-activated cytotoxic lymphocytes combined with
radiation and anticancer drugs, Eur J Cancer 36:2007-2017, 2000
12. 山本哲也,植田栄作,尾崎登喜雄:細胞傷害性リンパ球による癌細胞のアポトーシス誘導に関する検討−抗原特異的および非特異的リンパ球によるアポトーシスと活性酸素ならびにミトコンドリアとの関係について−,口腔組織培養 11:35-36,
2002
13. 山本哲也:アポトーシスのすべて,第10章リンパ球の細胞傷害作用とアポトーシス,3.LAK細胞,臨床免疫,38:250-257頁,科学評論社,東京,2002
14. Yamamoto
T, Kimura T, Ueta E, Tatemoto Y, Osaki T: Characteristic cytokine generation
patterns in cancer cells and infiltrating lymphocytes in oral squamous cell
carcinomas and the influence of chemoradiation combined with immunotherapy on
these patterns, Oncology 64:407-415, 2003
15.
Yamamoto T, Ueta E, Osaki T: Apoptosis induction
by interleukin-2-activated cytotoxic lymphocytes in a squamous cell carcinoma
cell line and Daudi cells−involvement of reactive oxygen species-dependent
cytochrome c and reactive oxygen species- independent apoptosis-inducing
factors, Immunology 110:217-224, 2003